Dr Sapna Patel
Paris – “Ce n’est pas seulement ce que vous donnez, c’est quand vous le donnez”, a déclaré l’investigateur rapportant “que le même traitement pour le mélanome résécable administré dans un ordre différent peut générer des taux plus faibles de récidive du mélanome”.
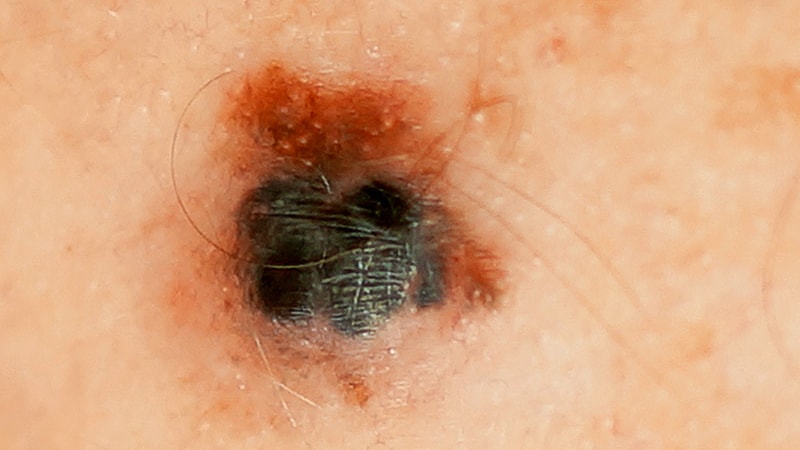
Sapna Patel, MD, professeur agrégé d’oncologie médicale du mélanome à l’Université du Texas MD Anderson Cancer Center, a rapporté les résultats de l’essai SWOG S1801, qui ont montré que les patients atteints de mélanome à haut risque qui ont reçu du pembrolizumab avant et après la chirurgie avaient beaucoup plus longtemps survie sans événement que les patients ayant reçu du pembrolizumab après chirurgie uniquement.
Après un suivi médian de près de 15 mois, le taux de récidive ou de décès était inférieur de 42 %.
“Par rapport au même traitement administré entièrement dans le cadre adjuvant, le pembrolizumab néoadjuvant suivi du pembrolizumab adjuvant améliore la survie sans événement dans le mélanome résécable”, a commenté Patel.
Elle a suggéré que l’explication des résultats était que “l’inhibition des points de contrôle immunitaires PD-1/PD-L1 avant la chirurgie donne une réponse antitumorale aux sites locaux et distants, et cela se produit avant la résection du lit tumoral. Cette approche tend à laisser derrière elle un plus grand nombre de lymphocytes T anti-tumoraux…[and] ces lymphocytes T peuvent être activés et diffusés systématiquement pour reconnaître et attaquer les tumeurs mélanomes micro-métastatiques. »
Les résultats ont été présentés ici lors d’un symposium présidentiel lors de la réunion annuelle 2022 de la Société européenne d’oncologie médicale (ESMO) à Paris, en France.
“Cet essai nous fournit plus de preuves sur le moment où une stratégie peut être préférée à l’autre”, a commenté Maya Dimitrova, MD, oncologue médicale au NYU Langone Perlmutter Cancer Center, New York. Elle n’a pas participé au procès.
« L’immunothérapie néoadjuvante a suscité des réponses pathologiques complètes impressionnantes, qui jusqu’à présent se sont avérées être associées à une réponse durable. Actualités médicales Medscape lorsqu’il est sollicité pour un commentaire.
“Comme pour toute thérapie néoadjuvante, nous ne voulons pas que le traitement compromette les résultats de la chirurgie lorsque l’intention est curative, et nous avons une fois de plus la preuve que ce n’est pas le cas en ce qui concerne l’immunothérapie”, a-t-elle déclaré. Cependant, elle a ajouté que “nous aurons besoin de données de survie supplémentaires pour vraiment changer la norme de pratique dans le mélanome à haut risque et démontrer s’il existe une séquence supérieure de traitement et de chirurgie”.
Détails des nouveaux résultats
L’essai clinique S1801 a recruté 345 participants atteints d’un mélanome de stade IIIB à IV considéré comme résécable. La cohorte a été randomisée pour recevoir soit une chirurgie initiale suivie de 18 doses de pembrolizumab 200 mg toutes les 3 semaines pour un total de 18 doses, soit un traitement néoadjuvant avec pembrolizumab 200 mg (3 doses) suivi de 15 doses de pembrolizumab adjuvant.
Le critère d’évaluation principal était la survie sans événement (EFS), définie comme le temps écoulé entre la randomisation et l’apparition de l’un des éléments suivants : progression de la maladie ou toxicité ayant entraîné la non-intervention chirurgicale, incapacité à commencer un traitement adjuvant dans les 84 jours suivant la chirurgie, mélanome récidive après chirurgie ou décès quelle qu’en soit la cause.
À un suivi médian de 14,7 mois, la SSE était significativement plus élevée pour les patients du groupe néoadjuvant par rapport à ceux recevant un traitement adjuvant uniquement (HR, 0,58 ; log-rank unilatéral P = 0,004). Au total, 36 participants sont décédés dans les groupes néoadjuvant et adjuvant (14 et 22 patients, extrapolant à un rapport de risque de 0,63 ; unilatéral P = 0,091).
“Avec un nombre limité d’événements, la survie globale n’est pas statistiquement différente pour le moment”, a déclaré Patel. “La survie historique à 2 ans était de 72 % dans le bras néoadjuvant et de 49 % dans le bras adjuvant.”
Les auteurs notent que le bénéfice du traitement néoadjuvant est resté constant pour toute une série de facteurs, notamment l’âge du patient, le sexe, l’état de performance, le stade de la maladie, l’ulcération et BRAF statut. La même proportion de patients dans les deux groupes a reçu du pembrolizumab adjuvant après la chirurgie.
Les taux d’événements indésirables étaient similaires dans les deux groupes, et le pembrolizumab néoadjuvant n’a pas entraîné d’augmentation des événements indésirables liés à la chirurgie. Dans le groupe néoadjuvant, 28 patients (21 %) ayant soumis des rapports pathologiques ont présenté une réponse pathologique complète (0 % de tumeur viable) lors de l’examen local.
Des questions demeurent
Le commentateur invité James Larkin, PhD, FRCP, FMedSci, chercheur clinique au Royal Marsden Hospital, Londres, Royaume-Uni, a noté que l’étude avait des “résultats frappants” et était un essai historique avec une conception simple mais puissante.
Cependant, il a souligné certaines questions qui devront être traitées à l’avenir. “Une question importante est quelle est la durée optimale d’un traitement néoadjuvant et peut-on l’individualiser ?”
Une autre question est de savoir combien de traitement postopératoire est vraiment nécessaire et la pathologie peut-elle aider à le déterminer. “Peut-on éviter complètement la chirurgie en toute sécurité?” Il a demandé. “Un autre problème est le besoin d’une thérapie anti-CTL4 – quels patients pourraient bénéficier d’anti-CTL4, en plus de l’anti-PD-1 ?”
“Et par extension, ce paradigme fournit une excellente plate-forme pour tester de nouveaux agents, y compris des combinaisons dans les cas où PD-1 n’est pas suffisant pour obtenir une réponse suffisante”, a déclaré Larkin. “À l’avenir, les essais portant sur ces questions nous offrent une opportunité majeure d’individualiser et de désamorcer rationnellement le traitement.”
Pesant également sur l’étude, un autre expert a souligné que la thérapie néoadjuvante dans ce contexte est déjà considérée comme une option. “L’utilisation de l’immunothérapie avant la chirurgie a été rapportée dans certains essais tels que les essais OPACIN-neo et PRADO”, a déclaré Anthony J. Olszanski, RPh, MD, vice-président de la recherche au Fox Chase Cancer Center, Philadelphie, PA. “Les résultats ont été assez excitants et ont conduit le NCCN à l’inscrire comme une option potentielle pour certains patients dans les directives actuelles sur le mélanome.”
Le S1801 est financé par le NIH/NCI et en partie par MSD dans le cadre d’un accord de recherche et de développement coopératif avec le NCI. Le pembrolizumab (KEYTRUDA) est Merck‘s thérapie anti-PD-1. Patel a déclaré de multiples relations avec l’industrie, comme indiqué dans le résumé ; plusieurs co-auteurs ont également fait des révélations. Olszanski a signalé avoir participé à des conseils consultatifs pour BMS, Merck et InstilBio et avoir mené des essais pour eux.
ESMO 2022. Résumé LBA6. Présenté le 11 septembre 2022
Roxanne Nelson est une infirmière autorisée et une rédactrice médicale primée qui a écrit pour de nombreux grands médias et contribue régulièrement à Medscape.
Suivez Medscape sur Facebook, TwitterInstagram et YouTube.