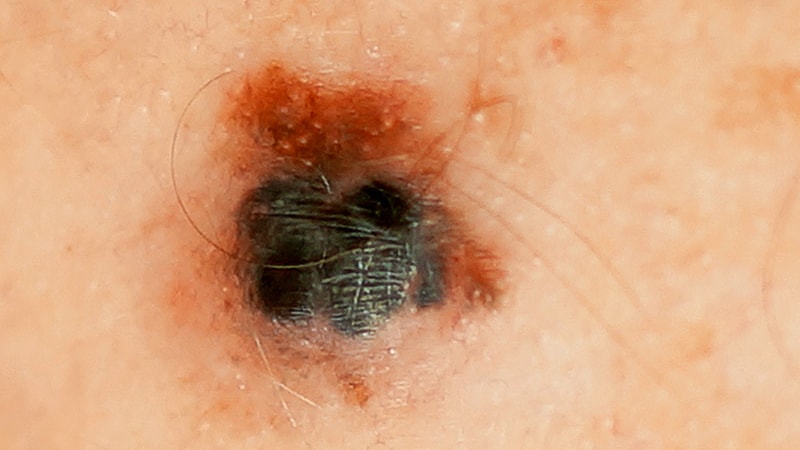
Une mutation dans un gène impliqué dans le remodelage de la chromatine est associée à un mélanome agressif, selon une nouvelle étude combinant des données in vitro et des modèles animaux.
Le gène, ARID2, fait partie du complexe switch/saccharose non fermentescible (SWI/SNF), qui manœuvre les structures cellulaires appelées nucléosomes pour rendre l’ADN cellulaire accessible. Environ 20 % des cancers humains présentent une mutation au sein du complexe SWI/SNF.
Dans la nouvelle étude, publiée dans Cell Reports, les chercheurs ont rapporté que la sous-unité ARID2 était mutée chez environ 13% des patients atteints de mélanome identifiés par le Cancer Genome Atlas.
Des mutations ARID2 ont été trouvées dans les lésions précoces du mélanome, ce qui, selon les auteurs, pourrait jouer un rôle dans la dissémination précoce des cellules cancéreuses. D’autres études ont montré des mutations SWI/SNF, y compris des mutations ARID2, dans les métastases du mélanome, en particulier au cerveau.
Les chercheurs ont également découvert une régulation à la hausse des voies synaptiques dans les cellules de mélanome ainsi que l’Atlas du génome du cancer, qui suggère également un rôle potentiel de la perte d’ARID2 dans les métastases ou le ciblage du cerveau, car il a été démontré ailleurs que l’activation synaptique dans les cellules cancéreuses influence migration et survie des cellules dans le cerveau.
“Nous attendons avec impatience les futures études qui étudient le rôle du complexe PBAF… afin de mieux adapter les traitements aux patients atteints de mélanome”, ont écrit les auteurs de l’étude, qui étaient dirigés par Emily Bernstein, PhD, professeure en sciences oncologiques au Icahn School of Medicine à Mount Sinai, New York.
Le complexe SWI/SNF comprend un sous-complexe qui cible des séquences d’ADN spécifiques ou des domaines de lecteur de chromatine. Il existe plusieurs versions du sous-complexe de ciblage, mais deux des plus fréquentes sont BAF et PBAF. La sous-unité la plus souvent mutée dans le mélanome est ARID2, qui fait partie du PBAF et contient une région riche en AT responsable des interactions ADN non spécifiques à la séquence. Il existe des preuves qu’il joue un rôle dans la suppression des tumeurs. Dans les tumeurs de souris, l’épuisement d’ARID2 est associé à une sensibilité accrue à l’inhibition du point de contrôle immunitaire et à la destruction par les lymphocytes T.
Pour mieux comprendre le rôle d’ARID2 dans la suppression des tumeurs, les chercheurs ont utilisé CRISPR-Cas9 pour créer un déficit en ARID2 dans une lignée cellulaire connue de mélanome métastatique humain. Ils ont découvert que l’accessibilité de la chromatine et l’expression des gènes qui l’accompagnaient étaient réduites parmi certains PBAF et les régions occupées par BAF-PBAF. Il y avait également une augmentation de l’accessibilité de la chromatine et de l’expression des gènes dans les régions occupées par le BAF, et ces changements étaient associés à l’agression tumorale. Chez la souris, ils ont conduit à des métastases des organes distaux.
Ce mécanisme semble être conservé entre différentes lignées cellulaires de mélanome, mais les cibles transcriptionnelles dérégulées étaient différentes selon les facteurs de transcription dominants dans la lignée cellulaire. Cela suggère que l’effet de la mutation ou de la perte d’ARID2 peut être différent selon le stade de progression du mélanome ou le niveau d’invasivité. “Comme le mélanome comprend des populations de cellules hétérogènes distinctes sur le plan de la transcription, nous envisageons de futures études utilisant des méthodologies unicellulaires pour mieux comprendre les effets nuancés de la perte d’ARID2 au sein de sous-populations de cellules dans les tumeurs du mélanome humain”, ont écrit les auteurs.
L’étude est limitée par le fait que toutes les mutations ARID2 n’entraînent pas une perte complète de protéines et peuvent plutôt conduire à des complexes aberrants.
L’étude a été financée par les National Institutes of Health.
Cet article a été initialement publié sur MDedge.com, qui fait partie du réseau professionnel Medscape.