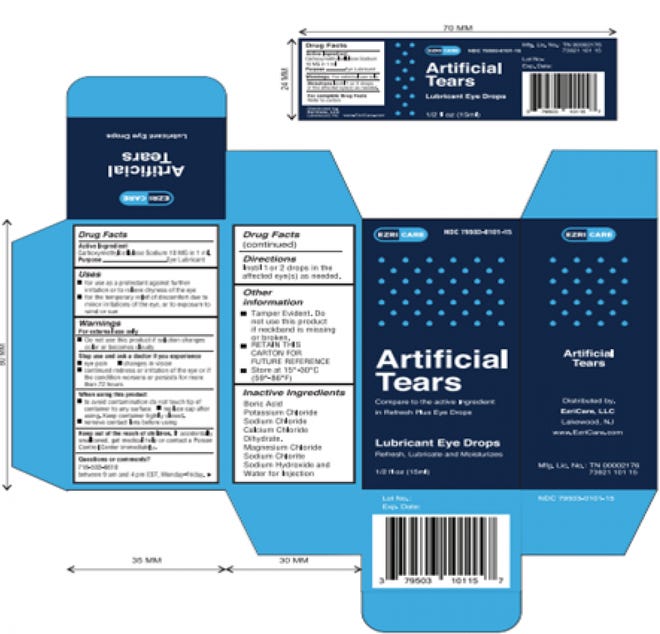
Un produit de larmes artificielles étudié par les Centers for Disease Control and Prevention a été rappelé en raison d’une possible contamination, de multiples infections et d’au moins un décès.
Global Pharma Healthcare fabrique les larmes artificielles EzriCare, qui ont été liées à un germe appelé pseudomonas aeruginosa.
La société a déclaré jeudi que tous les lots étaient rappelés.
Au moins 55 patients ont été touchés, souffrant d’infections oculaires, de cécité et d’un décès par infection du sang, a annoncé la société cette semaine.
Des cas ont été signalés dans au moins 12 États, dont la Californie, le New Jersey et la Floride. Les patients ont souffert d’une perte de vision permanente et au moins une personne est décédée d’une infection du sang, a déclaré le CDC dans une note du 20 janvier.
“Global Pharma Healthcare informe les distributeurs de ce produit, Aru Pharma Inc. et Delsam Pharma et demande aux grossistes, détaillants et clients qui possèdent le produit rappelé de cesser de l’utiliser”, a déclaré la société dans son annonce de rappel.
Poursuites : Quel est le procès contre CVS et Walmart ? Chaînes ciblées sur les ventes de produits homéopathiques
Rappels : Liste complète des rappels de la FDA depuis 2012
Le rappel intervient après une enquête du CDC et de la FDA sur une “épidémie multi-états d’une souche extrêmement résistante aux médicaments” d’une infection. La souche, VIM-GES-CRPA, est nouvelle aux États-Unis
“Pour le moment, le CDC recommande aux cliniciens et aux patients de cesser d’utiliser les produits EzriCare Artificial Tears en attendant des directives supplémentaires du CDC et de la FDA”, a déclaré le CDC sur son site Web.

Que dit EzriCare ?
EzriCare a déclaré sur son site Web que la société n’était au courant d’aucun test “liant définitivement” l’épidémie aux larmes artificielles d’EzriCare.
La société n’a pas reçu de plaintes de consommateurs liées à l’enquête.
“Nous avons immédiatement pris des mesures pour arrêter toute distribution ou vente de larmes artificielles EzriCare”, a écrit la société. “Dans la mesure du possible, nous avons contacté les clients pour les déconseiller de continuer à utiliser le produit.”
La société a déclaré que Global Pharma Healthcare PVT Limited fabrique le produit en Inde tandis qu’Aru Pharma Inc. importe le produit aux États-Unis.
“Le seul rôle d’EzriCare, LLC dans l’introduction du produit sur le marché était de concevoir une étiquette extérieure et de la commercialiser auprès de nos clients”, a déclaré la société, niant tout rôle dans la formulation, la conception du système de livraison de l’emballage ou la fabrication du produit en question. .
Quels états ont été impactés ?
Des patients ont été signalés dans :
- Californie
- Colorado
- Connecticut
- Floride
- New Jersey
- Nouveau Mexique
- New York
- Nevada
- Texas
- Utah
- Washington
- Wisconsin
Le CDC a déclaré que des échantillons avaient été prélevés entre mai 2022 et janvier 2023 et que la plupart des patients avaient utilisé des larmes artificielles. Les patients ont déclaré avoir utilisé 10 marques différentes de larmes artificielles, mais EzriCare était la marque la plus fréquemment signalée.
Les tests en laboratoire du CDC ont trouvé la souche VIM-GES-CRPA dans des flacons EzriCare ouverts provenant de plusieurs lots, a déclaré le CDC.
L’agence teste toujours des bouteilles non ouvertes de larmes artificielles EzriCare pour voir si une contamination s’est produite pendant la fabrication.
Quels sont les symptômes?
Le CDC a déclaré que les symptômes d’infection comprennent:
- Écoulement jaune, vert ou clair de l’œil
- Douleur ou gêne oculaire
- Rougeur de l’œil ou de la paupière
- Sensation de quelque chose dans l’œil (sensation de corps étranger)
- Sensibilité accrue à la lumière
- Vision trouble
J’ai utilisé les larmes artificielles EzriCare, que dois-je faire ?
Les patients doivent cesser d’utiliser les larmes artificielles EzriCare en attendant des informations supplémentaires du CDC et de la FDA, ont déclaré les agences.
“Les patients qui ont utilisé des larmes artificielles sans conservateur EzriCare et qui présentent des signes ou des symptômes d’infection oculaire doivent consulter immédiatement un médecin”, a déclaré le CDC. “Pour le moment, il n’y a aucune recommandation pour tester les patients qui ont utilisé ce produit et qui ne présentent aucun signe ou symptôme d’infection.”
Saleen Martin est journaliste dans l’équipe NOW de USA TODAY. Elle est de Norfolk, Virginie – le 757 – et aime tout ce qui concerne l’horreur, les sorcières, Noël et la nourriture. Suivez-la sur Twitter à @Saleen_Martin ou envoyez-lui un e-mail à [email protected].