Les conjugués anticorps-médicament (ADC) révolutionnent les soins prodigués aux patients atteints de certaines tumeurs solides avancées.
Actuellement, la FDA a approuvé six ADC pour traiter divers cancers solides, notamment ceux du sein, de l’estomac, du col de l’utérus et résistants au platine cancer des ovairesainsi que une autre poignée pour traiter une gamme d’hémopathies malignes, notamment lymphome. Les indications de ces médicaments continuent de s’étendre aux stades précoces de la maladie et des monothérapies aux thérapies combinées.
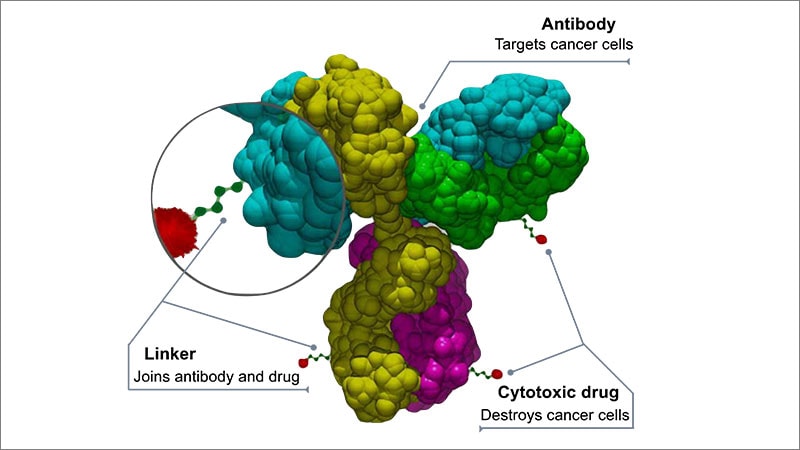
La justification de l’utilisation des ADC en oncologie est solide : concevoir un anticorps qui cible un antigène présent principalement dans les tumeurs mais pas dans les tissus normaux, relier cet anticorps à une charge utile cytotoxique et, essentiellement, créer une bombe intelligente capable de libérer sa fureur cytotoxique sur un cible spécifique. cible.
Mais, même avec cette conception ciblée, les ADC viennent souvent avec des effets secondaires puissants. Les complications graves comprennent la myélosuppression, la neuropathie périphérique, les infections, neutropéniethrombocytopénie, anémiefatigue, diarrhéedes nausées, des vomissements et des anomalies des enzymes hépatiques.
Compte tenu du nombre croissant de patients recevant des ADC et des indications croissantes de leur utilisation, comprendre les profils de toxicité de ces médicaments et développer des stratégies pour atténuer et gérer ces effets secondaires sont devenus primordiaux, Paolo Tarantino, MD, du Dana-Farber Cancer Institute. à Boston, et ses collègues ont expliqué dans un examen récent explorer les toxicités des ADC et les efforts visant à améliorer la sécurité des patients.
Dans le paysage de la toxicité
Une série de facteurs peuvent éclairer le type et la gravité des toxicités ADC qu’un patient peut ressentir.
En général, les toxicités associées aux ADC sont liées à leurs charges utiles de chimiothérapie, a expliqué Tarantino.
Les ADC sacituzumab govitecan (Trodelvy) et trastuzumab le deruxtécan (Enhertu), par exemple, incorpore tous deux un inhibiteur de la topoisomérase comme charge utile toxique. Les principales toxicités associées à ces agents – alopécie, neutropénie et diarrhée – correspondent aux toxicités observées avec les inhibiteurs de la topoisomérase non conjugués.
De même, le trastuzumab emtansine (Kadcyla), l’enfortumab vedotin (Padcev), le mirvetuximab soravtansine (Elahere) et le tisotumab vedotin (Tivdak), qui ont un inhibiteur de microtubules comme charge utile, présentent des toxicités similaires à celles des médicaments inhibiteurs de microtubules. Ces toxicités comprennent l’alopécie, la myélosuppression, la diarrhée et la neuropathie périphérique.
“Par conséquent, la sélection de la charge utile peut avoir des implications majeures sur le profil de toxicité attendu des ADC”, écrivent Tarantino et ses collègues dans leur revue.
Cependant, le lieur et l’anticorps peuvent également jouer un rôle dans le type, l’incidence et la gravité des toxicités des ADC.
L’anticorps, par exemple, peut entraîner des effets indésirables dus à ce que l’on appelle des toxicités ciblées et hors tumeur. Ces toxicités se produisent lorsque l’anticorps engage des cellules non malignes qui expriment la cible spécifique de l’ADC et provoquent l’accumulation de la charge utile sur ces sites.
Un exemple bien connu de toxicité ciblée et hors tumeur est la cardiotoxicité liée à l’ADC, qui peut survenir avec Médicaments ciblant HER2 qui utilise trastuzumab.
Des effets secondaires graves, potentiellement mortels, des ADC peuvent également survenir lorsque les molécules fabriquées libèrent leur charge toxique trop tôt, ou lorsque la toxine se diffuse non seulement dans le microenvironnement tumoral mais également dans les tissus en dehors de la région ciblée, provoquant ce qu’on appelle un Effet spectateur.
“L’effet spectateur est une arme à double tranchant”, a déclaré à Medscape Aditya Bardia, MD, MPH, du Massachusetts General Hospital à Boston. “Les nouveaux ADC ont un effet spectateur, ce qui, je pense, a beaucoup contribué à leur efficacité.” Cependant, a ajouté Bardia, “cela peut également provoquer une toxicité”.
Les ADC peuvent également présenter des toxicités particulières et moins prévisibles, a ajouté Tarantino.
Les patients qui reçoivent du trastuzumab déruxtécan, par exemple, peuvent développer maladie pulmonaire interstitielle, ce qui peut être fatal. C’est “probablement le plus important à retenir car cela signifie que le patient doit être surveillé très attentivement avec des tomodensitogrammes du thorax plus souvent qu’avec d’autres traitements”, a-t-il déclaré. Cependant, le mécanisme expliquant pourquoi certains patients développent cet événement indésirable reste flou.
Un autre problème, qui rend les événements indésirables plus difficiles à prévoir, est que « les médicaments ayant des cibles ou des charges utiles similaires n’ont pas toujours une toxicité identique », a déclaré Bardia.
L’ADC expérimental datopotamab deruxtecan (Dato-DXd) en est un exemple. Le datopotamab deruxtecan cible Trop2, tout comme le sacituzumab govitecan, et la charge utile est le deruxtecan, comme le trastuzumab deruxtecan, mais l’effet secondaire le plus courant du datopotamab deruxtecan est la mucite, quelque chose en général “que nous ne voyons pas avec le trastuzumab deruxtecan ou le sacituzumab govitecan”, Bardia expliqué. En d’autres termes, « c’est beaucoup plus complexe » que les seuls composants spécifiques de l’ADC.
Approches pour atténuer les toxicités
Compte tenu du large éventail de toxicités liées aux ADC, les experts ont exploré une multitude de stratégies pour améliorer la tolérabilité de ces agents.
Il s’agit notamment d’ajuster la chimie de l’anticorps, du lieur ou de la charge utile cytotoxique de l’ADC, d’explorer des stratégies de dosage optimisées dans le cadre des essais cliniques et d’identifier des biomarqueurs de toxicités chez les patients recevant des ADC pour aider à prédire et à gérer les événements indésirables plus tôt.
Bardia a expliqué que les toxicités inattendues apparues au cours des premiers essais cliniques ont aidé les cliniciens à développer des stratégies pour les atténuer. De telles stratégies comprennent la recherche fréquente de pneumopathie chez les patients recevant du trastuzumab deruxtecan, l’utilisation d’un bain de bouche prophylactique pour prévenir la mucite associée au datopotamab deruxtecan et, pour ceux recevant du sacituzumab govitecan, l’administration d’un facteur de stimulation des colonies de granulocytes pour prévenir la neutropénie, ainsi que l’administration aux patients lopéramide et des antiémétiques pour traiter la diarrhée et les nausées.
Trouver une dose optimisée pour chaque ADC est également crucial pour minimiser les événements indésirables, a noté Tarantino, citant les premières études sur le trastuzumab deruxtecan dans le traitement des tumeurs colorectales, pulmonaires et autres tumeurs solides dans lesquelles l’ADC, administré à 6,4 mg/kg, était efficace mais également hautement efficace. toxique.
“La FDA a exigé une étude randomisée pour comparer la dose de 6,4 mg/kg à la dose de 5,4 mg/kg, et des études sur le cancer colorectal et le cancer du poumon ont révélé que la dose de 5,4 était tout aussi efficace et moins toxique”, a-t-il déclaré.
Tarantino et ses collègues suggèrent également l’utilisation de biocapteurs portables pour identifier et gérer plus tôt les toxicités liées à l’ADC. De tels appareils pourraient, par exemple, fournir des données en temps réel sur la fréquence cardiaque, la respiration et même les niveaux de saturation en oxygène des patients afin d’identifier les premiers signes de maladie pulmonaire interstitielle.
Dans l’ensemble, « les innovations dans la conception des ADC, les tests pharmacogénomiques et les biocapteurs portables ainsi qu’une attention accrue portée à l’optimisation du dosage des ADC par le biais d’essais prospectifs dédiés pourraient aider à exploiter le potentiel de cette classe très prometteuse de médicaments anticancéreux, qui est encore loin d’être pleinement exploitée ». exploré”, écrivent Tarantino et ses collègues.
L’examen de Tarantino et de ses collègues n’a pas été financé. Tarantino a agi en tant que conseiller et/ou consultant pour AstraZeneca, Daiichi Sankyo, Gilead et Lilly. Bardia est consultant ou membre du conseil consultatif de Pfizer, Novartis, Genentech, Merck, Radius Health, Immunomedics/Gilead Sciences, Sanofi, Daiichi Sankyo, AstraZeneca et Eli Lilly, et a reçu un financement de recherche de Genentech, Novartis, Pfizer, Merck. , Sanofi, Radius Health, Immunomedics/Gilead Sciences, Daiichi Sankyo, AstraZeneca et Eli Lilly.
Neil Osterweil, journaliste médical primé, est un collaborateur fréquent et de longue date de Medscape.
Pour en savoir plus sur Medscape Oncology, rejoignez-nous sur X (anciennement Twitter) et Facebook