Parmi les patients atteints du syndrome auto-inflammatoire sévère récemment défini VEXAS, ceux qui sont dépendants d’une transfusion ou qui ont une substitution d’acides aminés spécifique sont les plus à risque de décès, tandis que ceux atteints de chondrite de l’oreille sont à risque significativement plus faible, a découvert une équipe multinationale de chercheurs.
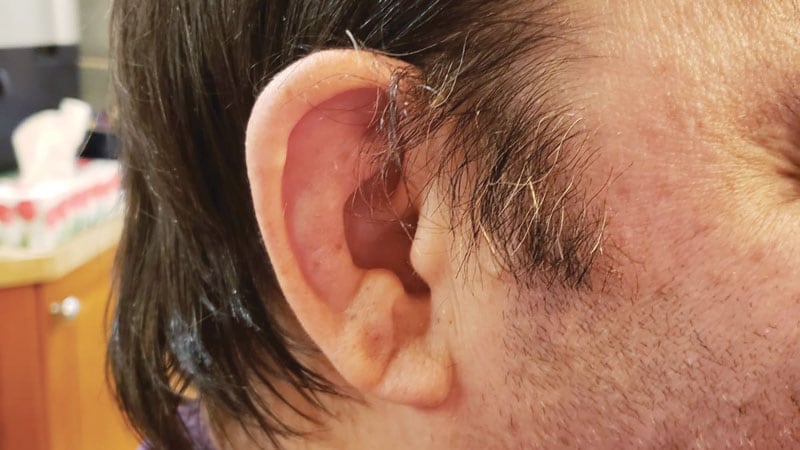
Chondrite auriculaire chez un homme atteint de VEXAS.
Leur étude de la mortalité et des prédicteurs de survie chez les patients atteints de VEXAS génétiquement confirmé a montré que les patients présentant une variante du VEXAS entraînant une substitution d’acides aminés d’une méthionine à une valine avaient un risque de décès 3,5 fois plus élevé que les patients présentant soit une méthionine- substitution en thréonine ou un échange méthionine en leucine.
La dépendance transfusionnelle était un prédicteur indépendant de la mortalité. Les patients qui sont devenus dépendants des transfusions après l’apparition des symptômes présentaient un risque de décès presque trois fois plus élevé, a rapporté Marcela A. Ferrada, MD, chercheuse clinique à l’Institut national de l’arthrite et des maladies musculo-squelettiques et cutanées (NIAMS).
“Ces résultats devraient éclairer l’évaluation des risques et la gestion clinique chez les patients atteints du syndrome VEXAS”, a-t-elle déclaré dans une présentation orale d’un résumé lors de la réunion annuelle 2021 de l’American College of Rheumatology (ACR), qui s’est tenue en ligne.
“Ces découvertes génétiques se sont avérées actuellement non seulement diagnostiques, mais nous avons montré qu’elles sont également pronostiques, et nous espérons que cela nous aidera à identifier les patients qui pourraient avoir un traitement plus agressif”, a déclaré Ferrada.
Elle a également discuté de ses conclusions lors d’une conférence de presse tenue 2 jours avant sa présentation plénière. Lors de ce briefing, Actualités médicales Medscape ont demandé aux cliniciens participants s’ils avaient des patients qu’ils soupçonnaient d’avoir un VEXAS non diagnostiqué.
“Ma réponse est intéressante”, a répondu le modérateur Vaneet Sandhu, MD, de l’Université de Loma Linda, à Loma Linda, en Californie, et du Riverside University Health System.
“Au cours des deux derniers jours, j’ai lu des articles sur le VEXAS et j’ai en fait envoyé un texto à un de mes collègues hier pour lui dire:” Hé, vous connaissez ces patients que nous avons vus qui ont ces étranges éruptions cutanées et chondrites et ont peut-être un diagnostic de vascularite leucocytoclasique ou autre ne diagnostiquons-nous pas ces patients ? » ” elle a dit.
“Je pense que nous examinons chaque patient atteint de chondrite et réexaminons son phénotype. Nous avions rejeté certains symptômes car ils ne correspondaient pas à l’archétype de la polychondrite récurrente, par exemple, mais cela pourrait être le VEXAS”, a déclaré Alfred Kim, MD, PhD , de la Washington University School of Medicine, à St. Louis, Missouri, qui a également présenté des données lors du briefing.
Trois variantes
Le VEXAS est causé par des mutations somatiques dans UBA1, un gène qui initie l’ubiquitylation cytoplasmique, un processus par lequel les protéines mal repliées sont marquées pour la dégradation.
Le nom du syndrome est un acronyme décrivant les principales caractéristiques :
-
Vacuoles dans les cellules de la moelle osseuse
-
E-1 enzyme activatrice qui UBA1 encode pour
-
X-lié
-
UNEauto-inflammatoire
-
Smutation omatique caractérisée par un mosaïcisme hématologique
Le VEXAS entraîne des symptômes rhumatologiques, dermatologiques et hématologiques qui sont souvent diagnostiqués à tort comme étant causés par une polychondrite récurrente réfractaire au traitement, une périartérite noueuse, un syndrome de Sweet, une artérite à cellules géantes ou un syndrome myélodysplasique (SMD).
Le VEXAS a été identifié comme un syndrome distinct au cours de la dernière année par Ferrada et d’autres chercheurs du NIAMS, du National Human Genome Research Institute et d’autres institutions.
Dans l’étude rapportée à l’ACR 2021, Ferrada et ses collègues ont évalué 83 hommes qui avaient été référés pour des tests génétiques pour le VEXAS aux National Institutes of Health, à Bethesda, Maryland, et au Leeds Teaching Hospitals NHS Trust, à Leeds, Royaume-Uni.
Il a été confirmé que tous les patients présentaient des mutations génétiques définissant le VEXAS dans UBA1 par séquençage Sanger d’échantillons de sang périphérique. Seuls les patients présentant des mutations au niveau du codon p.Met41 ont été inclus dans l’analyse des investigateurs. Les mutations sur ce site représentent presque tous les cas de VEXAS qui ont été identifiés à ce jour.
La manifestation clinique la plus courante du VEXAS était l’atteinte cutanée, qui s’est produite chez tous les 83 patients sauf un. Les autres manifestations courantes comprenaient l’arthrite (58 patients), les infiltrats pulmonaires (57 patients) et la chondrite de l’oreille (54 patients).
Quinze patients présentaient la variante leucine, 18 la variante valine et 50 la variante thréonine. L’âge médian au début de la maladie était de 66 ans dans les groupes variants leucine et thréonine et de 65 ans dans le groupe variant valine.
Le diagnostic clinique différait selon le génotype : 4 des 18 patients (22%) avec le variant valine ont reçu un diagnostic de polychondrite récurrente, contre 8 sur 15 (53%) avec le variant leucine et 31 sur 50 (62%) avec le thréonine une variante (P = .01).
En revanche, 55% des patients avec le génotype valine ont été diagnostiqués avec une fièvre indifférenciée, contre 6% de ceux avec le génotype leucine et 16% avec les génotypes thréonine (P = .001). Plus de patients avec le variant leucine (60 %) ont reçu un diagnostic de syndrome de Sweet, contre 11 % et 14 % des patients avec les variants valine et thréonine, respectivement (P = .001).
Il n’y avait pas de différence significative entre les trois génotypes dans le pourcentage de patients diagnostiqués avec le SMD.
La période de suivi variait de 1 à 18 ans (médiane, 4,7 ans). La durée médiane de survie depuis le début de la maladie pour tous les patients était de 10 ans.
Parmi les patients avec le variant valine, la survie médiane était de 9 ans, ce qui était significativement moins que chez les patients avec les deux autres variants (P = .01).
En analyse univariée, les prédicteurs indépendants de mortalité étaient la chondrite de l’oreille (hazard ratio [HR], 0,26 ; P = 0,005), la dépendance transfusionnelle, une variable dépendante du temps (HR : 2,59 ; P = 0,03) et la variante valine (HR, 3,5 ; P = .008).
L’association entre le génotype et le phénotype VEXAS pourrait s’expliquer par la découverte que parmi les patients avec la variante valine, il y avait significativement moins de traduction du catalytiquement compétent. UBA1b isoforme que les patients avec les deux autres variantes, a déclaré Ferrada.
Options thérapeutiques
Ferrada a noté qu’à ce jour, aucun médicament ne s’est avéré apporter des avantages thérapeutiques constants pour les patients atteints de VEXAS, mais des preuves quant à l’étiologie du syndrome indiquent des approches thérapeutiques possibles.
“Je pense que toutes ces découvertes sont extrêmement importantes pour nous aider à guider la prise en charge de ces patients, car nous savons que la mutation est localisée dans les cellules souches de la moelle osseuse. Nous soupçonnons donc que faire une greffe de moelle osseuse chez ces patients va être curatif », a déclaré Ferrada lors du briefing.
Les chercheurs prévoient un essai de phase 2 de greffe allogénique de cellules souches hématopoïétiques pour les patients atteints de VEXAS.
L’étude a été soutenue par les National Institutes of Health. Ferrada, Sandhu et Kim n’ont révélé aucune relation financière pertinente.
Réunion annuelle 2021 de l’American College of Rheumatology (ACR) : Résumé 1426. Présenté le 8 novembre 2021.
Neil Osterweil, journaliste médical primé, est un contributeur de longue date et fréquent de Medscape.
Pour plus d’actualités, suivez Medscape sur Facebook, Twitter, Instagram et YouTube.
.

:quality(85)/cloudfront-us-east-1.images.arcpublishing.com/infobae/2LVZ56S3GVCMJPPH3O6OIEG4V4.jpg)







